細胞内において自己・非自己の境界線を決定する分子パターンの発見
~自己由来成分の病原体含有液胞をセルオートノマス免疫系が捕捉するメカニズムの解明~
東京薬科大学・生命科学部・感染制御学研究室の新崎恒平教授らのグループは、大阪大学微生物病研究所・山本雅裕教授と笹井美和准教授、岐阜大学大学院医学系研究科・永井宏樹教授と久堀智子准教授、京都大学大学院医学研究科・中川一路教授と野澤孝志准教授らのグループとの共同研究により、感染宿主の自己成分である細胞膜によって覆われたレジオネラ含有液胞膜が細胞内において非自己としてセルオートノマス免疫系に捕捉される仕組みを解明しました。本研究の成果は、セルオートノマス免疫系が自己成分を「非自己」として識別できる分子機構の一端を明らかにしたとともに、この仕組みの解析はセルオートノマス免疫系に由来する自己免疫疾患発症機構の理解に繋がることが期待されます。
本成果は、米国National Academy of Sciencesが刊行する科学誌「Proceedings of the National Academy of Sciences of the United States of America」に掲載されました。
【研究成果のポイント】
・ 宿主由来の細胞膜で覆われたレジオネラ含有液胞(Legionella-containing vacuole; LCV)へのセルオートノマス免疫系関連分子であるGBP の集積には、レジオネラの病原因子であるLpg2552 が必要であることを明らかにしました。
・ Lpg2552 はLCV 膜においてリン脂質のホスファチジン酸の合成を促進していることを発見するとともに、GBP がこのホスファチジン酸の集積を非自己のサインとして識別することでLCV 膜を破壊していることを見出しました。さらに、ホスファチジン酸を認識できないGBP の変異体はLCV 膜を捕捉できず、その結果、レジオネラの細胞内増殖を抑制できないことを明らかにしました。
・ これらの成果は、GBP による他の病原体含有液胞に対する攻撃メカニズムの研究の一助となる他、GBP が関わる自己免疫疾患の発症機構を解明する足掛かりとなることが期待されます。
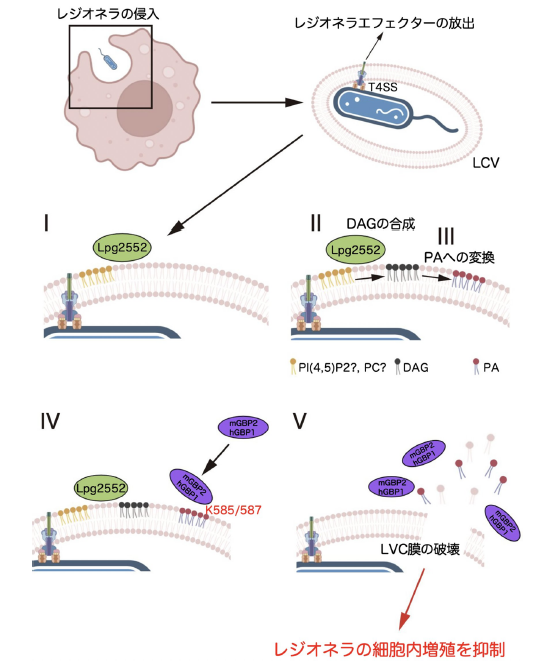
研究概略図
詳しい研究成果(和文)はこちら
書誌情報
| 雑誌名 | Proceedings of the National Academy of Sciences of the United States of America |
|---|---|
| 論文タイトル |
Phosphatidic acid production on the vacuole harboring Legionella pneumophila is a signal for recognition of interferon-induced GTPases |
| 著者 |
Hiromu Oide, Tomoko Kubori, Hiroki Nagai, Takashi Nozawa, Ichiro Nakagawa, Miwa Sasai, Masahiro Yamamoto, Kohei Arasaki |
| DOI | https://doi.org/10.1073/pnas.2420096122 |
